涉三四五批國采和48個品種!廣州牽頭13省國采續采
發布時間:2024-11-08 10:53:45 閱讀量:834
作者:醫藥慧 來源:醫藥慧
核心提示:今日,廣州交易集團有限公司、廣州公共資源交易中心發布《關于征求《廣東聯盟阿哌沙班等藥品集中帶量采購文件(征求意見稿)》意見的通知》,征求意見時間2024年11月7日至2024年11月12日18:00。
今日,廣州交易集團有限公司、廣州公共資源交易中心發布《關于征求《廣東聯盟阿哌沙班等藥品集中帶量采購文件(征求意見稿)》意見的通知》,征求意見時間2024年11月7日至2024年11月12日18:00。
根據梳理,本次接續采購由廣州GPO組織實施聯盟采購,聯盟范圍有13個省份,包括安徽、福建、江西、湖北、湖南、廣東、重慶、四川、云南、西藏、陜西、甘肅、新疆。品種范圍則是國家集采第三、四、五批采購協議期滿的 48 個品種,包括阿哌沙班、阿那曲唑等品種。(詳見附件)
采購周期原則上不超過兩年,自中選結果實際執行日起計算,首年采購期截止至 2025 年 12 月 31 日。具體執行時間和采購周期以聯盟省(區)公布為準。
申報品種條件
屬于本次集中帶量采購藥品范圍,并于報名截止之日(含)前獲得國內有效注冊批件且滿足以下要求之一的上市藥品,應具備相應批件或可在國家藥品監督管理局藥品評審中心《化學藥品目錄集》中查詢到相應結果:
1. 國家藥品監督管理部門發布的仿制藥質量和療效一致性評價參比制劑。
2.通過國家藥品監督管理部門仿制藥質量和療效一致性評價的仿制藥品。
3.根據《國家食品藥品監督管理總局關于發布化學藥品注冊分類改革工作方案的公告》(2016 年第 51 號)或《國家藥監 局 關 于 發 布 化 學 藥 品 注 冊 分 類 及 申 報 資 料 要 求 的 通 告 》(2020 年第 44 號),按照化學藥品注冊分類批準,并證明質量和療效與參比制劑一致的仿制藥品。
在采購年度內完成協議采購量后,公立醫療機構(含未報量的公立醫療機構)仍應優先采購使用中選產品,中選產品總使用量(含公立醫療機構最終確認中選限量產品的協議采購量)占同品種同組藥品總使用量的比例不低于 70%。
中選辦法
擬中選分不限量企業和限量企業以擬中選企業P的“單位可比價”由低到高順位排序依次確定擬中選不限量企業。其余擬中選企業為擬中選限量企業。
擬中選企業數量要求
不限量企業:首年采購期100%的預采購量,并同時獲得增量資格以及待分配量的分配資格
限量企業:首年采購期60%的預采購量,該部分量由醫療機構最終確認,剩余預采購量額歸入待分配量,并且不具備待分配量的分配資格。
分配量辦法
聯盟省(區)醫療機構應在規定時間內按中選結果于國家招采子系統(廣東)調整并確認待分配量與協議采購量,具體如下所示:
(1)聯盟省(區)醫療機構需選擇是否采購中選限量產品,若確認選擇獲得中選限量資格的原報量產品,醫療機構需在國家招采子系統(廣東)進行確認,該部分采購量為首年預采購量的 60%。對于該中選限量產品剩余的首年預采購量,醫療機構需新增中選不限量產品對其進行分配,直至分配完畢并最終確認協議采購量。
(2)若聯盟省(區)醫療機構確認不選擇獲得中選限量資格的原報量產品,醫療機構需在國家招采子系統(廣東)重新選擇采購中選不限量產品,并同步確定中選不限量產品的協議采購量。
(3)若聯盟省(區)醫療機構原報量產品未中選,醫療機構需在國家招采子系統(廣東)重新選擇采購中選產品,并按上述第(1)(2)點分配首年采購期預采購量。(點擊“閱讀原文”查看)
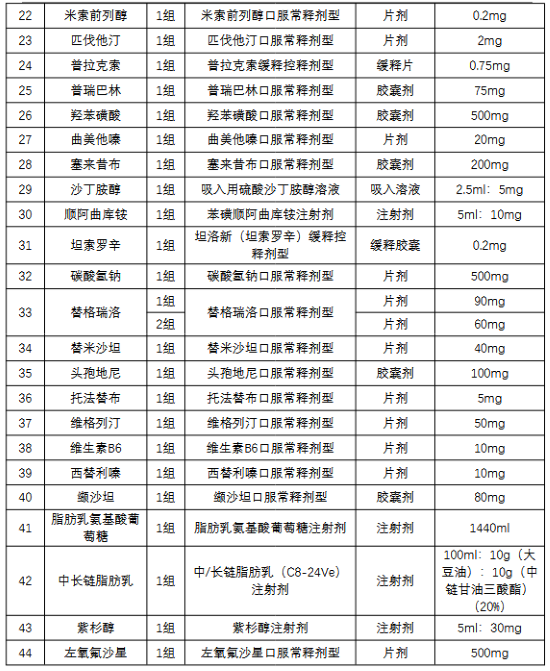
附件.48個藥品采購清單及統一代表品